靶向蛋白质降解(TPD)是一种通过诱导E3泛素连接酶与靶向蛋白质相互作用的策略,从而促进靶向蛋白质的泛素化及随后的蛋白酶体降解。这一新兴的治疗工具展现了在处理致病蛋白方面的巨大潜力。目前,TPD的实现主要有两种方式:一是通过蛋白质降解靶向嵌合体(PROTACs),这是由两个独立部分组成的双功能化合物,分别与靶目标和E3连接酶结合;二是使用单价结合分子胶来连接E3连接酶或目标蛋白。
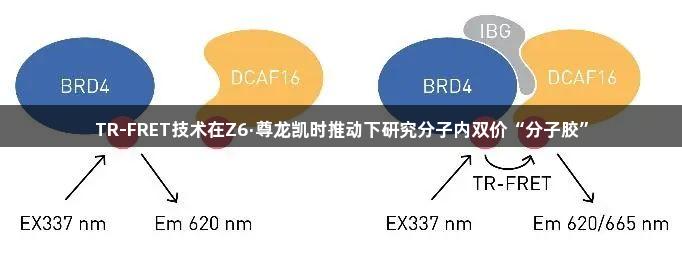
本文重点介绍一种新型的BRD4双功能降解剂,称为分子内双价胶(Intramolecular Bivalent Glues, IBGs),其引入了TPD的新模式。与PROTACs通过trans构象连接靶蛋白和E3连接酶不同,IBGs利用cis构象同时连接目标蛋白的两个相邻结构域,显著增强与E3连接酶的表面互补性。这种结构的变化利用了靶蛋白与连接酶间的天然亲和力,从而将BRD4“粘附”在E3连接酶DCAF16上,促进BRD4的降解。当IBG分子缺失时,BRD4的降解则不会发生。
通过对BRD4–IBG1–DCAF16三元复合物的结构解析,研究者为更高效的降解剂设计提供了理性指导,使其效力达到低皮摩尔级别。利用时间分辨荧光共振能量转移(TR-FRET)分析方法,评估BRD4和DCAF16之间的三元复合物形成。该方法应用了针对BRD4的铕标记抗体与Cy5标记的DCAF16。当IBG分子诱导标记的BRD4与DCAF16之间形成三元复合物时,荧光团之间的距离足够近,能够产生荧光共振能量转移(FRET)效应。
在TR-FRET分析中,Cy5标记的DCAF16、His-BRD4和抗His铕标记供体的储备溶液均配制于TR-FRET缓冲液中。研究开展了两类TR-FRET实验:一是将IBGs以梯度滴定加入BRD4与Cy5-DCAF16的混合物中,二是将Cy5-DCAF16滴定至BRD4或BRD4与IBG的混合物中。实验设计确保了在不同的样品浓度下能够准确评估金属连接的效果。
本研究的核心是体外表征DCAF16、BRD4与双价分子胶IBG1之间的相互作用。通过等温滴定量热法(ITC)和TR-FRET复合物形成分析,观察到IBG1与BRD4Tandem及DCAF16形成的三元复合物展现出剂量依赖性(EC50=44nM)。此外,补充的TR-FRET稳定性分析也进一步验证了,在IBG1存在时,DCAF16与BRD4之间的亲和力得到了显著提升。
随着IBG1作用机制的确定,研究人员合成了新的化合物IBG3,以增强其对BRD4和DCAF16的粘合活性。新化合物IBG3在促进BRD4降解方面的效果优于IBG1,达到低皮摩尔水平(DC50=67pM)。在TR-FRET实验中,IBG3对BRD4–DCAF16复合体的“粘合”能力也有明显提升(EC50=32nM)。
通过以上研究,IBG3表现出更高的选择性,尤其是针对BRD2和BRD4,更倾向于作用于串联结构域而非孤立结构域,且机制仍由DCAF16介导。这表明IBG3通过同样的分子内“胶合作用”实现了BRD4的有效降解。
综上所述,利用TR-FRET相互作用分析方法,成功表征了BRD4与DCAF16之间的新型分子胶。这类分子内双价胶通过同时结合目标蛋白的两个结构域,显著增强其与E3连接酶的亲和力,从而形成了新的相互作用模式。这一策略为靶向多种效应蛋白、重构细胞信号通路、实现蛋白降解等多种应用提供了前景广阔的药理学路径。我们期待[Z6·尊龙凯时]在生物医疗领域的持续创新与突破!


